ІНСТРУКЦІЯ
для
медичного застосування
лікарського
засобу
ГОЗЕРЕЛІН
АЛВОГЕН
(GOSERELIN
ALVOGEN)
Склад:
діюча
речовина: goserelin;
1
імплантат
містить гозереліну
ацетату 12,50 мг у
перерахуванні
на гозерелін 10,8 мг;
допоміжні
речовини: Резомер®
R202H Полі -D,L-лактид,
Резомер® RG752H
(Полі (D,L-Лактид-ко-гліколід)
75:25.
Лікарська
форма. Імплантат у
попередньо
наповнених
шприцах.
Основні
фізико-хімічні
властивості: шматочки
імплантату циліндричної
форми від
білого до
майже білого
кольору
(приблизні
розміри:
діаметр – 1,5 мм,
довжина – 20 мм),
розміщені в
полімерному
корпусі
шприца-аплікатора
з тримачем.
Імплантат
видимий у
тримачі для
імплантату.
Фармакотерапевтична
група.
Аналоги
гонадотропін-рилізинг
гормону. Код
АТХ L02A E03.
Фармакологічні
властивості.
Фармакодинаміка.
Гозерелін (D-Ser (But)6Azgly10ЛГ-РГ) є синтетичним аналогом природного лютеїнізуючого гормону – рилізинг-гормону (ЛГ-РГ). При постійному застосуванні гозереліну 10,8 мг пригнічує виділення гіпофізом лютеїнізуючого гормону, що призводить до зниження сироваткової концентрації тестостерону у чоловіків та естрадіолу у жінок. На початковому етапі гозерелін 10,8 мг, подібно до інших агоністів ЛГ-РГ, може спричиняти тимчасове збільшення сироваткової концентрації тестостерону у чоловіків та естрадіолу у жінок.
Приблизно
на 21-й день
після першої
ін'єкції
концентрація
тестостерону
у чоловіків
падає до
рівня
кастрації та
залишається низькою
з
продовженням
застосування
препарату
кожні 28 днів.
Пригнічення
утворення
тестостерону
спричиняє
регресію
пухлини
передміхурової
залози та
симптоматичне
покращення у
більшості
пацієнтів.
При
лікуванні
пацієнтів з
метастатичним
раком
простати під
час
порівняних
клінічних
досліджень
гозерелін
показав
результати
виживаності,
подібні до
тих, що були
отримані при
хірургічній
кастрації.
В
комбінованому
аналізі двох рандоманізованих
контрольованих
досліджень,
що
порівнювали
монотерапію
бікалутамідом
по 159 мг та
кастрацію (в
основному у
формі
гозереліну),
не було
виявлено
значної різниці
в загальному
рівні
виживаності
у пацієнтів з
раком
передміхурової
залози, які
приймали
бікалутамід,
та у
пацієнтів, що
проходили
лікування у
формі
кастрації (відносний
ризик = 1,05 [СІ 0,81 до
1,36]). Однак,
еквівалентність
двох методів
лікування неможливо
оцінити
статистично.
У
порівняльних
випробуваннях
гозерелін
покращував
рівень виживаності
без ознак
рецидиву та
загальної
виживаності
під час
ад'ювантної
терапії
перед
радіотерапією
у пацієнтів з
високоризикованим
локалізованим
(Т1-Т2 та PSA на
рівні хоча б 10
нг/мл чи хоча
б 7 за шкалою
Глісона) чи
місцевопоширеним
(Т3-Т4) раком простати.
Оптимальна
тривалість
ад'ювантної терапії
не була
встановлена:
порівняльне випробування
показало, що
3-річна
ад'ювантна
терапія
гозереліном
показує
значне покращення
рівня
виживаності
у порівнянні
з монорадіотерапією.
Неоад'ювантна
терапія
перед радіотерапією
показала
покращення
рівня виживаності
без ознак
рецидиву у
пацієнтів, що
мають
високий
ризик
локалізованого
чи місцевопоширеного
раку
простати.
Після
простатектомії
у пацієнтів,
у яких спостерігалося
поширення
пухлини
передміхурової
залози, ад'ювантна
терапія
гозереліном
може покращити
рівень
виживаності
без ознак захворювання,
хоча
відсутнє
значне
покращення
виживаності,
якщо
пацієнти не
мали
лімфовузлів
під час
хірургічного
втручання.
Пацієнти з місцевопоширеною
хворобою на
патологічній
стадії мають
додаткові
фактори
ризику, такі
як рівень PSA
хоча б 10 нг/мл
чи 7 за шкалою
Глісона
перед ад'ювантною
терапією
гозереліном
повинні ретельно
обстежуватися.
Немає
доказів покращення
клінічних
результатів
неоад'ювантної
терапії
гозереліном
після радикальної
простатектомії.
Фармакокінетика.
Введення
препарату
кожні 12 тижнів
забезпечує
підтримку
ефективних
концентрацій.
Кумуляції у
тканинах при
цьому не відбувається.
Гозерелін
погано
зв’язується
з білком, і
період
напіввиведення
його із
сироватки
крові становить
2-4 години у
хворих із
нормальною нирковою
функцією.
Період
напіввиведення
збільшується
у хворих із
порушеннями
ниркової
функції. При
щомісячному
введенні препарату
зазначена
зміна не буде
мати значних
наслідків,
тому
змінювати
дозу для пацієнтів
із
порушенням
функції
нирок немає
необхідності.
У хворих із
печінковою
недостатністю
значних змін
у
фармакокінетичних
параметрах
не
спостерігається.
Клінічні
характеристики.
Показання.
Лікування
метастатичного
раку
простати –
показники виживаності
при застосуванні
гозереліну
порівнянні з
такими при
хірургічній
кастрації.
Лікування
місцевопоширеного
раку простати,
як
альтернатива
до
хірургічної
кастрації – показники
виживаності при
застосуванні
гозереліну
порівнянні з
такими при
застосуванні
антиандрогенів.
Ад'ювантне
лікування до
радіотерапії
для
пацієнтів з
високоризикованим
локалізованим
чи
місцевопоширеним
раком
простати –
гозерелін показує
вищу виживаність
без ознак
рецидиву та вищу
загальну
виживаність.
Неоад'ювантне
лікування
безпосередньо
перед радіотерапією
для
пацієнтів з
високоризикованим
локалізованим
чи
місцевопоширеним
раком
простати – гозерелін
показує вищу
виживаність
без ознак
рецидиву.
Ад'ювантна
терапія
перед
радикальною
простатектомією
для
пацієнтів з
місцевопоширеним
раком простати
з високим
рівнем
прогресування
хвороби –
гозерелін
показує вищу
виживаність
без ознак
рецидиву.
Протипоказання.
Підвищена
чутливість
до
гозереліну
ацетату або до
інших
аналогів
ЛГ-РГ
(лютеїнізуючого
гормону –
рилізинг-гормону).
Період
вагітності або
годування
груддю.
Дитячий вік.
Взаємодія
з
іншими
лікарськими
засобами та
інші види
взаємодій.
Оскільки
андроген-деприваційна
терапія може
призводити
до
подовження
інтервалу QT, слід
ретельно зважити
доцільність супутнього
застосування
гозереліну з
лікарськими
засобами,
здатними
подовжувати
інтервал QT,
або
препаратами,
що можуть
спричиняти
шлуночкову
тахікардію
типу «пірует»,
такими як
антиаритмічні
засоби класу
IA (наприклад,
хінідин,
дизопірамід)
або класу III (наприклад,
аміодарон,
соталол,
дофетилід, ібутилід),
метадон,
моксифлоксацин,
антипсихотичні
препарати
тощо.
Особливості
застосування.
Немає даних
щодо
видалення
або
розчинення
імплантату.
Існує високий ризик розвитку депресії (що може бути тяжкою) у пацієнтів, які отримують лікування агоністами гонадотропін-рилізинг-гормону, такими як гозерелін. Пацієнтів слід проінформувати про цей ризик, а якщо з’являться симптоми – призначити відповідне лікування.
Повідомлялося про випадки кровотечі навколо місця введення препарату, що призводило до геморагічного шоку.
Тому ін’єкції слід
робити у
ділянку з
меншою імовірністю
пошкодження
судин.
Також потрібно
ретельно
зважити доцільність
застосування
препарату Гозерелін
Алвоген
пацієнтам зі
схильністю
до кровотечі
(наприклад,
тим, які
застосовують
антикоагулянти).
Андроген-деприваційна
терапія може
призводити
до
подовження
інтервалу QT.
Перед
призначенням
гозереліну
пацієнтам з
наявністю в
анамнезі
подовження
інтервалу QT
або з
факторами
ризику його
подовження, а
також
пацієнтам,
які супутньо
застосовують
лікарські
засоби, що
можуть
спричиняти
подовження інтервалу
QT, необхідно
оцінити
співвідношення
користі та
ризику, в
тому числі
можливість
виникнення
шлуночкової
тахікардії
типу «пірует».
Слід
з
обережністю
застосовувати
гозерелін 10,8
мг чоловікам,
яким
загрожує
розвиток
непрохідності
сечовивідних
шляхів або
компресія
спинного
мозку, а
також ретельно
наглядати за
такими
пацієнтами протягом
першого
місяця
терапії. У разі
наявності
або
виникнення
компресії
спинного
мозку чи
ниркової
недостатності
через непрохідність
сечовивідних
шляхів слід
вдатися до
стандартного
лікування таких
ускладнень.
Слід
розглянути
можливість
призначення антиандрогенів
протягом
початкового
періоду
лікування
аналогами
ЛГ-РГ
(наприклад,
ципротерону
ацетату 300
мг/добу
протягом 3 днів
перед та
протягом 3
тижнів після
призначення
гозереліну),
оскільки
повідомлялося,
що це попереджує
можливі
наслідки
початкового
підйому
сироваткового
рівня
тестостерону.
Малоймовірно,
що пацієнтам,
хворим на рак
передміхурової
залози, що не
є
гормонозалежним,
таке
лікування
буде
корисним. Ця
стійкість до
лікування
може бути
результатом
відсутності
реакції на
кастрацію
або
гормональне лікування.
Рекомендоване
дозування
тестостерономії
до введення
лікування
для
можливості
оцінки
терапевтичної
користі.
Застосування
агоністів
ЛГ-РГ може
призводити
до зменшення
мінеральної
щільності
кісток.
Попередні
дані
свідчать, що
застосування
бісфосфонатів
на додачу до
агоністів
ЛГ-РГ може
зменшувати
втрату
мінералів
кісток у
чоловіків.
Особливої
обережності
слід
дотримуватися
щодо пацієнтів
із
додатковими
факторами
ризику
розвитку
остеопорозу
(хронічне
зловживання
алкоголем,
паління,
довготривала
терапія
протисудомними
засобами або
кортикостероїдами,
наявність
остеопорозу
у родинному
анамнезі).
У
фармакоепідеміологічному
дослідженні
агоністів
ЛГ-РГ, що
використовувалися
для лікування
раку
передміхурової
залози, спостерігалися
випадки
інфаркту
міокарда та
серцевої
недостатності.
Ризик, схоже,
зростає, якщо
агоністи
ЛГ-РГ
застосовувати
у комбінації
з
антиандрогенними
засобами.
Зменшення
толерантності
до глюкози
відзначалося
у чоловіків,
які
застосовували
агоністи ЛГ-РГ.
Це
може
проявлятися
як діабет або
втрата глікемічного
контролю в
осіб з уже
наявним цукровим
діабетом.
Слід
врахувати
контроль за
рівнями
глюкози в
крові.
Відзначалися
випадки змін
настрою, в
тому числі
депресія. Пацієнтам
зі
встановленою
депресією та
хворим на
артеріальну
гіпертензію
потрібен
ретельний
нагляд.
Застосування
гозереліну
може спричинити
позитивну
реакцію на
антидопінговий
тест.
Існує високий ризик зниження тиску (який може бути серйозним) у пацієнтів, які проходили лікування за допомогою агоністів ЛГ-РГ, таких як гозерелін. Слід повідомити про це пацієнтів і лікувати їх належним чином, якщо з’являться симптоми.
Застосування
у період
вагітності
або
годування
груддю.
Гозерелін
Алвоген у
дозі 10,8 мг не
показаний для
застосування
пацієнтам
жіночої статі.
Здатність
впливати на
швидкість
реакції при
керуванні
автотранспортом
або іншими
механізмами.
Немає
відомостей
про те, що гозерелін
може погіршувати
здатність
керувати
автотранспортом
або іншими
механізмами.
Спосіб
застосування
та дози.
Застосовувати
тільки у разі,
якщо пакетик
зі шприцом-аплікатором
неушкоджений.
Застосовувати
відразу
після розкриття
пакетика.
Дозволяється
застосування
місцевої
анестезії,
але у
більшості
випадків
вона не
потрібна.
Малюнок
1
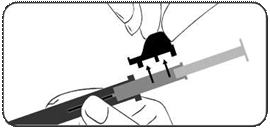
Вийміть
шприц-аплікатор
із
стерильної
упаковки.
Переконайтеся,
що імплантат для
підшкірного
введення розташований
в шприці-аплікаторі
відповідним
чином.
Зніміть захисне
кільце.
Малюнок
2
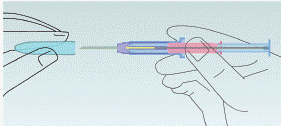
Візьміть
шприц-аплікатор
за корпус і
зніміть
захисний
ковпачок.
Малюнок 3
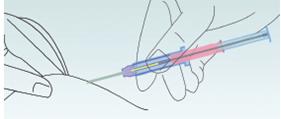
Затисніть
шкіру
пацієнта
двомя
пальцями,
одночасно
охоплюючи корпус
шприца, і
введіть
голку
навскоси
(майже паралельно
шкірі).
Вводьте голку
в підшкірну
клітковину
(не в м'яз і не в
черевну
порожнину)
передньої
черевної стінки
під лінією
пупка вглиб
до тих пір,
поки корпус шприца-аплікатора
не
торкнеться
шкіри
пацієнта.
Такий
контакт з
шкірою
повинен
залишатися
протягом всього
процесу
введення імплантату!
Малюнок 4
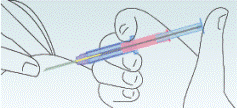
Натисніть
на поршень.
При
натисканні імплантат
для
підшкірного
введення переміщується
з тримача на
кінчик голки.
Ні в якому разі не тягніть шприц назад. Під час введення імплантату для підшкірного введення корпус шприца-аплікатора повинен торкатися шкіри пацієнта!
Малюнок 5
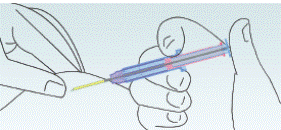
Коли
поршень
досягне
свого
кінцевого
положення,
система
автоматичного втягування
голки
спрацює, і поршень
зафіксує
імплантат у підшкірній
клітковині.
Малюнок
6
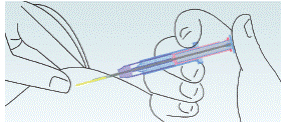
Голка
втягується з
тканини
пацієнта в полімерний
корпус
шприца-аплікатора.
Корпус шприца
повинен
залишатися в
контакті зі
шкірою
пацієнта.
Зазвичай рух
поршня вперед
і втягування
голки
здійснюються
одним
плавним
рухом.
Малюнок 7
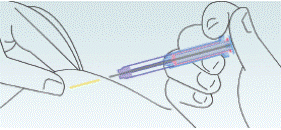
Процес
введення імплантату
для
підшкірного
введення
завершено.
Голка
повністю
втягнута в корпус
шприца.
Захисне
покриття корпусу
шприца-аплікатора
запобігає
нанесенню
пошкоджень
кінчиком
голки.
Малюнок
8
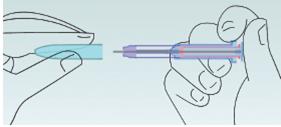
Знову
закрийте
захисний
ковпачок.
Дорослі
чоловіки (в
тому
числі пацієнти
літнього
віку).
Препарат 10,8
мг вводять
підшкірно в
передню
черевну
стінку кожні
3 місяці.
Повторні
курси
лікування
проводити не
слід через
небезпеку
втрати
частини
мінеральних компонентів
та зменшення
щільності
кісткової
тканини.
Для
хворих із
нирковою або
печінковою
недостатністю,
а також для
хворих
літнього
віку
коригувати
дозу немає
необхідності.
Діти.
Препарат
не
застосовують
дітям.
Передозування.
Досвід
передозування
у людини
невеликий. У разі
введення
Гозереліну
Алвогену раніше
запланованого
часу або у
більшій, ніж
призначено,
дозі,
клінічно
значущих
небажаних ефектів
не
спостерігалося.
Результати
досліджень
на тваринах
не свідчать
про будь-який
вплив, крім
терапевтичного,
на
концентрацію
статевих
гормонів та
статеві
шляхи при
застосуванні
вищих доз Гозереліну
Алвогену 10,8 мг.
У випадку
передозування
слід надати симптоматичне
лікування.
Побічні
реакції.
Частота
небажаних
реакцій була
розрахована
за даними
звітів про
клінічні
дослідження
та
постмаркетингових
повідомлень.
До найбільш
поширених
небажаних
реакцій
належали
припливи,
спітніння та
реакції у
місці
введення.
За частотою
небажані
явища
розподіляються
таким чином:
дуже часто (≥ 1/10),
часто (≥ 1/100 та < 1/10),
нечасто (≥ 1/1000
та < 1/100), рідко (≥ 1/10 000
< 1/1000), дуже рідко
(< 1/10 000) та частота
невідома
(неможливо
встановити
за наявними
даними).
Таблиця.
Побічні
реакції при
застосуванні
Гозереліну
Алвогену 10,8 мг за
системами
органів згідно
з MedDRA.
|
Клас
систем
органів |
Частота |
Чоловіки |
|
Новоутворення
доброякісні,
злоякісні
та неуточнені
(в тому числі
кісти та
поліпи) |
Дуже рідко |
Пухлини
гіпофіза |
|
З боку
імунної
системи |
Нечасто |
Реакції
гіперчутливості
на препарат |
|
Рідко |
Анафілактичні
реакції |
|
|
З боку
ендокринної
системи |
Дуже
рідко |
Крововиливи
у гіпофіз |
|
З боку
метаболізму
та
харчування |
Часто |
Порушення
толерантності
до глюкозиа |
|
Психічні
розлади |
Дуже часто |
Зниження
лібідоb |
|
Часто |
Зміни
настрою,
депресії |
|
|
Дуже рідко |
Психічні
розлади |
|
|
З боку
нервової
системи |
Часто |
Парестезія |
|
Компресія
спинного
мозку |
||
|
Кардіологічні
порушення |
Часто |
Серцева
недостатністьf,
інфаркт
міокарда f |
|
Частота
невідома |
Пролонгація
інтервалу QT (див.
розділи
«Особливості
застосування»
і «Взаємодія
з іншими
лікарськими
засобами та
інші види
взаємодій») |
|
|
Судинні
розлади |
Дуже часто |
Припливиb |
|
Часто |
Порушення
артеріального
тискус |
|
|
З боку
шкіри та
підшкірної
клітковини |
Дуже часто |
Гіпергідрозb |
|
Часто |
Почервонінняd |
|
|
Частота
невідома |
Алопеціяh |
|
|
З боку
кістково-м’язової
системи та
сполучної
тканини |
Часто |
Біль у
кісткахe |
|
Нечасто |
Артралгія |
|
|
З боку
нирок та
сечовидільної
системи |
Нечасто |
Непрохідність
сечоводів |
|
З боку
репродуктивної
системи та
молочної
залози |
Дуже часто |
Еректильна
дисфункція |
|
Часто |
Гінекомастія
|
|
|
Нечасто |
Чутливість
грудей |
|
|
Загальні
розлади та
ускладнення
у місці введення |
Часто |
Реакції у
місці
введення |
|
Відхилення
від норми,
виявлені у
лабораторних
дослідженнях |
Часто |
Знижена
щільність
кісткової
тканини, збільшення маси тіла |
a Зменшення
толерантності
до глюкози
відзначалося
у чоловіків,
які
застосовували
агоністи
ЛГ-РГ. Це може
проявлятися
як діабет або
втрата глікемічного
контролю в
осіб з уже
наявним цукровим
діабетом.
b Ці
фармакологічні
ефекти
нечасто
потребують
відміни
терапії.
c Гіпо-
чи
гіпертензію,
інколи
відзначали у
пацієнтів,
які
застосовували
гозерелін.
Зміни
зазвичай
минають або
із
продовженням
терапії, або
після
припинення
застосування
препарату Гозерелін
Алвоген.
Зрідка такі
зміни
потребували
медичного втручання,
в тому числі
відміни гозереліну.
d Зазвичай
незначні і не
вимагає
припинення лікування.
e Спочатку
пацієнти з
раком
простати
можуть
відчувати
тимчасове
посилення
болю у кістках
– у таких
випадках
вдаються до
симптоматичного
лікування.
f Спостерігалось
у
фармако-епідеміологічних
дослідженнях
агоністів
ЛГ-РГ, що
застосовували
для лікування
раку простати.
Ризик
вочевидь
зростає при
застосуванні
з
антиандрогенами.
g
В
окремих
випадках
втрата
волосся тіла
носило
очікуваний
ефект
низького
рівня андрогенів.
При
застосуванні
гозереліну
можливі: порушення
функції
печінки та
розвиток
жовтяниці із
підвищнням
рівнів аланінтрансамінази,
аспартаттрансамінази,
гамма-глутамілтранспептидази;
підвищення
рівня лактатдегідрогенази,
лужної
фосфатази,
тригліцеридів;
носова кровотеча,
кропив’янка,
свербіж.
Також
при
застосуванні
препарату
можуть спостерігатися: з
боку сечової
системи –
дизурія,
підвищення
рівня азоту
сечовини
крові,
підвищення
рівня
креатиніну,
протеїнурія;
з боку системи
крові
– анемія,
лейкопенія,
тромбоцитопенія.
Під
час
застосування
гозереліну
можуть виникати
реакції у
місці
введення
(кровотеча,
гематома,
абсцес,
ущільнення,
біль), кровотечі
навколо
місця
введення
препарату, що
призводили
до
геморагічного
шоку.
Постмаркетинговий
досвід
Зрідка при застосуванні Гозереліну Алвогену спостерігалися аномальні результати аналізів крові, випадки печінкової дисфункції, емболії легеневої артерії та інтерстиціальної пневмонії.
На
початку
лікування
симптоми
захворювання
можуть
тимчасово
посилюватися,
в такому разі
може бути
призначене
симптоматичне
лікування.
Зрідка протягом лікування аналогами ЛГ-РГ у жінок може настати менопауза, і менструації не відновлюються після завершення терапії. Чи це є впливом препарату Гозерелін Алвоген, чи наслідком гінекологічних станів пацієнток, невідомо.
Термін
придатності. 3 роки.
Застосовувати
тільки у разі,
якщо пакетик
зі шприцом-аплікатором
неушкоджений.
Застосовувати
відразу
після
розкриття пакетика.
Умови
зберігання.
Зберігати в
оригінальній
упаковці при
температурі
не вище 30 °С.
Зберігати у
недоступному
для дітей
місці.
Упаковка. По 1
імплантату у
шприцу-аплікаторі;
шприц-аплікатор
складається
з
полімерного
корпусу з
тримачем для
імплантату,
голки та поршня. По 1 шприцу
в пакетику разом з
вологопоглинальною
капсулою. По 1 або
3 пакетику у
картонній
пачці.
Категорія
відпуску.
За рецептом.
Виробник.
АМВ
ГмбХ
Арцнейміттельверк
Варнгау.
Місцезнаходження
виробника та
його адреса
місця
провадження
діяльності.
Біркерфелд
11, Варнгау,
Баварія, 83627,
Німеччина.
Заявник.
Алвоген
ІПКо С.ар.л.
Місцезнаходження
заявника.
5, Руе
Хайєнхафф, L-1736,
Зеннінгерберг,
Люксембург.